|
Fondazione FONAMA |
fonama@fonama.org |
Tel. 335250742 |
 |
 |
Traduzioni a cura di Natale Marzari
Dopo 41 anni e 5 mesi, nel maggio 2006 la
magistratura di Trento ha riconosciuto l'esistenza e la gravità di quella
malattia rara che nessuna altra istituzione o persona singola della provincia di
Trento ancora mi riconosce, e per negare la quale ancora mi perseguita.
Natale Marzari |
Sistemi di trasporto mitocondriale
Le normali operazioni della catena respiratoria creano un differenziale di pH ed un gradiente di voltaggio di 30.000.000 volt/metro fra i due lati della membrana mitocondriale interna.
Questo richiede proteine di trasporto altamente specializzate per il controllo dei movimenti dei piccoli ioni attraverso la membrana, e la prevenzione della dissipazione dei vari
gradienti.
La maggior parte dei portatori interni della membrana sono
antiportatori che scambiano una molecola per un altra. Se le
cariche elettriche
sulle due molecole si equilibrano esattamente lo
scambio sarà un processo elettricamente neutro ed il potenziale
enorme della membrana non avrà effetto sul risultato. Tuttavia, il gradiente pH può interessare la posizione di equilibrio
di uno
scambio elettricamente neutro se uno o più partecipanti sono acidi
o basici.
I simportatori i trasportano due molecole nello stesso senso. Se le molecole hanno
cariche opposte questo può ancora essere un
processo elettricamente neutro. È sperimentalmente difficile da distinguersi fra
un simporto di
protone e un antiporto di idrossile.
Se le cariche delle molecole trasportate differiscono per
i
simportatori o gli antiportatori, allora ci sarà un
processo elettrico di trasporto (a volte
denominato elettrogenico). Tali portatori inscatolano "il sentire"
del
potenziale di
membrana, e ciò avrà un'influenza importante sul risultato. In generale i
gradienti influenzati dal componente pH della
forza motrice protonica sono ragionevolmente modesti, ma quelli influenzati dal
potenziale della membrana sono notevoli.
In molto pochi casi (per es. per l'assorbimento del calcio) il portatore
permette
semplicemente che lo ione caricato attraversi la membrana. Ciò costituisce un
uniportatore elettrico (o electrogenico). Il potenziale di membrana
esercita pienamente il suo effetto, conducendo a gradienti di concentrazione
notevoli se la reazione
potesse raggiungere l'equilibrio.
I sistemi principali di trasporto sono elencati nella tabella qui
sotto, la quale mostra inoltre alcuni degli inibitori principali.
|
portatore
|
stechiometria
|
inibitori
|
commenti
|
| fosfato |
scambio elettricamente neutro di
H2PO4-
for OH-
|
NEM
mersalile |
tutti i mitocondri |
| dicarbossilato |
scambio elettricamente neutro casuale
di
malato2- con succinato2-
o HPO42- |
malonato di
mersalile |
tutti i mitocondri |
| tricarbossilato |
scambio elettricamente neutro di
(citrato3- + H+ ) con malato2-
|
benzene 1,2,3
tricarbossilato |
tessuto adiposo mammifero
e fegato: serve per la
biosintesi degli acidi grassi |
| ossoglutarato |
scambio elettricamente neutro di
malato2- con ossoglutarato2-
|
_
|
la maggior parte dei tessuti
dei mammiferi ne abbisogna
per il
ciclo malato - aspartato |
adenina
nucleotide |
scambio elettrico ATP4-/ADP3-
|
atrattilosido
acido
bongcrecico |
tutti i mitocondri |
| glutammato |
scambio elettricamente neutro di
glutammato- con OH-
|
_
|
fegato dei mammiferi:
necessario
per il ciclo dell'urea |
| aspartato |
scambio elettrico di
(glutammato- + H+ ) con aspartato- |
_
|
la maggior parte dei tessuti di
mammiferi abbisognano per il
ciclo malato - aspartato |
| calcio |
uniportatore elettrico per il Ca++ |
_
|
sistema di assorbimento del calcio |
| calcio |
scambio elettricamente neutro di
Ca++ con 2H+ |
_
|
calcio mitocondriale
sistema di esportazione nel fegato |
calcio /
sodio
|
scambio elettricamente neutro di
Ca++ con 2Na+ |
_
|
calcio mitocondriale
sistema di esportazione nel cuore |
sodio /
protone |
scambio elettricamente neutro di
Na+ con H+ |
_
|
ampiamente distribuito
|
Lo squilibrio della carica associato al portantore adenina nucleotide porta ad una grande differenza
nel rapporto ATP/ADP fra la matrice ed il citosol. L'ATP ha effettivamente "una
parola in più" nel citosol,
perché la coppia ATP:ADP è mantenuta più lontana dall'equilibrio:
Le cellule tuttavia, non ottengono qualcosa per niente. Il trasporto dell'ATP,
dell'ADP ed il fosfato attraverso la membrana
mitocondriale interna costa un 33% di energia addizionale, sopra il minimo richiesto per la sintesi del
ATP
all'interno del compartimento della matrice mitocondriale. Questa energia
supplementare deve essere assicurata dalla catena
respiratoria. Un protone ulteriore è usato per alimentare entrambi
questi sistemi di
trasporto: la carica positiva di questo singolo protone alimenta lo scambiatore del
nucleotide adenina, mentre la sua alimenta l'assorbimento del
fosfato. I componenti pH ed elettrici della
forza motrice protonica sono
sfruttati separatamente.
Recentemente c'è stato un grande interesse verso la
proteina portatrice ATP:ADP come possibile auto-antigene nella
cardiomiopatia dilatativa, una malattia cardiaca comune e
debilitante. Questo stesso enzima è coinvolto nella transizione
di permeabilità mitocondriale
e nella apoptosi.
L'alto ATP/ADP citosolico implica una concentrazione
citosolica molto bassa di AMP, come conseguenza dell'equilibrio della miochinasi.
Ciò permette al 5' AMP di servire da segnale di emergenza, quale indica una
minaccia al rifornimento di ATP. Vari enzimi chiave (considerevolmente fosforilasi del
glicogeno e la fosfofructochinasi) sono fortemente attivati dalle basse
concentrazioni di 5'AMP. Questo nucleotide inoltre agisce sull'adenosina che
stimola il flusso di sangue ai tessuti attivi. Si noti che 5'AMP differisce da 3'5 'ampère ciclico
prodotto dall'adenile
ciclasi.
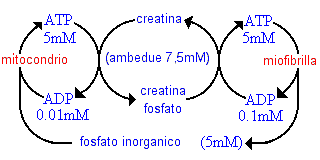
| La contrazione del muscolo richiede apparentemente un
rapporto molto alto di ATP/ADP, ed è difficile mantenere un basso ADP miofibrillare perché non
si diffonderà abbastanza rapidamente di nuovo ai mitocondri a bassi
livelli di ADP. (Il tasso di diffusione è direttamente proporzionale alla
concentrazione dei metaboliti.) I muscoli attivi contengono la
fosfochinasi della creatina,
(CPK) e grandi quantitativi di creatina e di fosfato di creatina. Queste
sostanze si
equilibrano con i gruppi del nucleotide adenina. Si pensa che le alte
concentrazioni di queste fonti di energia
altamente diffusibili aumentino il tasso massimo di trasporto di
energia. |
 |
Gli esperimenti di knockout del gene hanno indicato che i
topi che
difettano sia degli isoenzimi mitocondriali che miofibrillari di CPK
esibiscono uno sviluppo anormale, tuttavia i mutanti carenti in soltanto un
isoenzima sono apparentemente
sani. È difficile da vedere perché entrambi i geni del CPK dovrebbero
essere
ampiamente mantenuti se non fanno nulla. Rimane essere stabilito se i
singoli mutanti possono effettuare un lavoro sostenuto come quello del tipo di
controllo.
Uno dei trasportatori asimmetrici più importanti è il
portatore dell'aspartato, quale nei mammiferi gioca un ruolo chiave nella ri-ossidazione del
NADH glicolitico dal ciclo malato-aspartato. Questo ciclo è necessario
perché la membrana interna non è
permeabile a NAD o al NADH. Le reazioni componenti devono girare due volte per
ogni molecola di
glucosio ossidata dalla cellula. I due enzimi in questione, la malato deidrogenasi (MDH) e la
ossaloacetato transaminasi
del glutammato (GOT) sono fra il più attivi nel corpo. Entrambi gli enzimi
esistono nelle varianti mitocondriali e citosolica, ma tutte e quattro le proteine sono codificate dai geni nucleari.
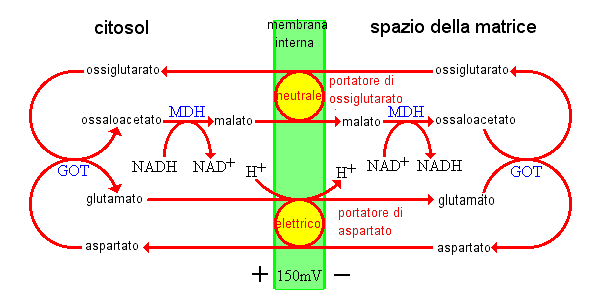
Viene scambiato l'aspartato con glutammato più un protone, così
la forza motrice protonica è applicata
interamente al portatore
dell'aspartato. L'effetto generale deve influenzare questo ciclo altrimenti
simmetrico, e mantenere il compartimento citosolico in uno stato relativamente "ossidativo" (con un
basso rapporto NADH/NAD) mentre lo
scompartimento mitocondriale è mantenuto corrispondentemente
ridotto. Questa disposizione sopprime la formazione del
lattato durante la
glicolisi aerobica. Le specie invertebrate impiegano le spole alternative per
realizzare
lo stesso effetto, ed è dubbioso se le cellule eucariotiche potessero affatto funzionare
senza una tale disposizione.
È importante rendersi conto che nessun portatore non significa
nessun
trasporto. Ossaloacetato e fumarate, per esempio, si legano molto male
al portatore dicarbossilato, e non sono trasportati ad alcun tasso
significativo. Se sia il malato che l'ossaloacetato fossero trasportati sarebbe
impossibile mantenere il differenziale redox per le NADH/ NAD che esiste fra
lo spazio matriciale mitocondriale ed il
citosol.
I geni del portatore del metabolita sono situati nel nucleo e
sono espressi soltanto in quei tessuti che li richiedono. Per esempio, i mitocondri del
fegato hanno portatori per ornitina e citrullina, i quali sono richiesti per il
ciclo dell'urea, ma questi non si ritrovano in altri tessuti. Il
portatore del citrato viene trovato soltanto nelle cellule e
negli adipociti del fegato, dove è necessario per la lipogenesi
Il risultato di molti esperimenti di ossidazione del substrato
in vitro è determinato dalla specificità del portatore. Per esempio: la maggior
parte dei mitocondri animali ossidano il succinato almeno quanto il malato, perché nè il fumarato nè
l'ossaloacetato possono essere esportati nella matrice e non c'è fonte di acetil-CoA per
produrre il citrato.
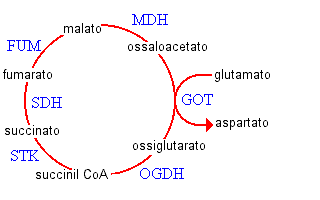 Anche
nei mitocondri del fegato, i quali possiedono un antiportatore del glutammato/idrossile, il glutammato
è aggiunto solo principalmente dall'aspartato
reso via transaminasi dell'ossaloacetato del glutammato
(GOT), dalla deidrogenasi dell'ossoglutarate (OGDH), dalla tiochinasi del succinato
(STK), dalla deidrogenasi del succinato (SADH), dalla fumarasi (FUM), dalla deidrogenasi del
malato (MDH) e dal portatore dell'aspartato.
Anche
nei mitocondri del fegato, i quali possiedono un antiportatore del glutammato/idrossile, il glutammato
è aggiunto solo principalmente dall'aspartato
reso via transaminasi dell'ossaloacetato del glutammato
(GOT), dalla deidrogenasi dell'ossoglutarate (OGDH), dalla tiochinasi del succinato
(STK), dalla deidrogenasi del succinato (SADH), dalla fumarasi (FUM), dalla deidrogenasi del
malato (MDH) e dal portatore dell'aspartato.
Tuttavia, se il glutammato ed il malato sono aggiunti insieme, i mitocondri
mammiferi inizialmente producono un ammontare uguale
dell'aspartato e dell'ossoglutarato usando la metà mitocondriale del
ciclo malato - aspartato. I portatori dell'ossoglutarato e dell'aspartato,
GOT, MDH e la catena respiratoria sono gli unici enzimi coinvolti in queste
circostanze.
Domanda di autovalutazione: Se i mitocondri fossero incubati
solo con ossoglutarato, quali vie sarebbero attive e quali composto (o composti)
verrebbe
formato?
In alcuni casi, per es. per gli ioni calcio, viene
utilizzato un portatore elettrico per l'assorbimento e viene usato un
sistema elettricamente neutro per l'esportazione. I due componenti
della forza motrice del protone sono usati per
spingere lo ione in due direzioni opposte. Ciò può essere sfruttata dalle cellule per
regolare il calcio intra-mitocondriale ad un valore differente dalla concentrazione citosolica..
Molti metaboliti importanti mostrano una distribuzione asimmetrica
attraverso la membrana interna mitocondriale. Il funzionamento dei
portatori elettricamente neutri
dell'anione porta ad una modesta accumulazione di acidi polibasici
(particolarmente citrato) all'interno dello spazio della matrice. Nel calcolo della
distribuzione di equilibrio, è soltanto la "linea inferiore"
che conta - il numero netto di
protoni che ha attraversato la membrana e quali procedure per
accumulare l'anione. Il meccanismo dettagliato è irrilevante, e tutti gli
"scambi" intermedi sono scontati. Se la reazione generale per accumulazione
elettricamente neutra del
metabolita è:
anionen-(out) + nH+(out)
<=> anionen-(in) + nH+(in)
allora una semplice considerazione sulle azioni di massa
porta a concludere che:
[anionen-in ] / [anionen-out
] = ([H+out] / [H+in])n
Ciò è utile per il funzionamento del ciclo dell'acido
citrico, ed inoltre ha implicazioni per la regolazione di glicolisi e della
lipogenesi dalla fosfofruttochinasi e dalla acilCoA carbossilasi, dove il citrato è un effettore allosterico..
Esperimenti di gonfiamento mitocondriale: Se si
vuole studiare il trasporto
della membrana nell'isolamento
è spesso necessario bloccare ulteriore il metabolismo con cianuro o rotenone. Gli studi più
accurati sulla cinetica di trasporto coinvolgono la
separazione veloce dei mitocondri dal loro mezzo di incubazione usando
l'ultrafiltrazione o la centrifugazione attraverso l'olio a base di
silicone. Questi esperimenti complessi e che richiedono tempo richiedono i
tracciatori radioattivi per correggere "l'apporto" del mezzo di
incubazione nella frazione mitocondriale. Movimenti del metabolita su grande scala, tuttavia, producono alterazioni nel volume della
matrice
attraverso i
meccanismi osmotici. Una valutazione qualitativa dei tassi di trasporto può
essere
ottenuta così misurando i cambiamenti nella dispersione della luce in
una sospensione mitocondriale torbida.
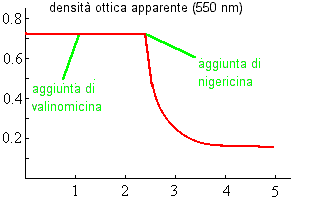 |
Questi risultati sono stati ottenuti da 0.5
mg di mitocondri del fegato sospesi a pH 7 in una provetta dello spettrofotometro con 2.5
ml a 150 mM di acetato di potassio. Gli ioni dell'acetato possono
penetrare velocemente tramite un
processo elettricamente neutro come acido acetico libero, ma nessun gonfiamento
è osservato inizialmente perché il potassio
non può entrare. L'aggiunta di valinomicina non ha effetto perché questo
ionoforo
catalizza il movimento elettrico. La Nigericina permette uno scambio elettricamente
neutro di ioni del
potassio per i protoni ed avviene il gonfiamento veloce.
|
Il gonfiamento passivo nelle soluzioni saline isotoniche dell'ammonio
può essere usato per studiare i sistemi principali di trasporto
dell'anione nei mitocondri bloccati dal cianuro. I soluti abbassano passivamente
i loro gradienti elettrochimici. Gli ioni dell'ammonio penetrano velocemente
come ammoniaca libera
senza movimento di carica, ed il gonfiamento è osservato se l'anione inoltre
è trasportato
tramite un processo elettricamente neutro. Può essere mostrato che il fosfato,
il malato, lo succinato, l'ossoglutarato, il citrato ed il sodio tutto sono presi
tramite
meccanismi elettricamente
neutri, ed possono essere dimostrati gli scambi fosfato/idrossile, fosfato/dicarbossilato, dicarbossilato/
tricarbossilato ed il malato/ossoglutarato.
È inoltre possibile osservare il "gonfiamento energetico"
usando
mitocondri intatti in cui i soluti sono accumulati contro il gradiente di concentrazione usando l'energia proveniente da respirazione o dal ATP esterno. Ci sono differenze notevoli fra i processi
energetici e passivi, ma in ogni caso (tranne le pompe alimentate dall'ATP) i
movimenti netti degli ioni sono sempre lungo il gradiente
elettrochimico.




 Anche
nei mitocondri del fegato, i quali possiedono un antiportatore del glutammato/idrossile, il glutammato
è aggiunto solo principalmente dall'aspartato
reso via transaminasi dell'ossaloacetato del glutammato
(GOT), dalla deidrogenasi dell'ossoglutarate (OGDH), dalla tiochinasi del succinato
(STK), dalla deidrogenasi del succinato (SADH), dalla
Anche
nei mitocondri del fegato, i quali possiedono un antiportatore del glutammato/idrossile, il glutammato
è aggiunto solo principalmente dall'aspartato
reso via transaminasi dell'ossaloacetato del glutammato
(GOT), dalla deidrogenasi dell'ossoglutarate (OGDH), dalla tiochinasi del succinato
(STK), dalla deidrogenasi del succinato (SADH), dalla 